من الأبحاث إلى العلاج: التقدُّم في فهم وعلاج اعتلال عضلة القلب التضخُّمي في الكويت
الكشف عن طفرات وارتباطات جديدة في اعتلال عضلة القلب التضخمي

بروفايل د. فريدة الحبيب
المؤهِّلات الأكاديمية
• حاصلة على درجتَي الماجستير والدكتوراه في طب القلب والأوعية الدموية الإكلينيكي من كلية الطب الملكية للدراسات العليا التابعة لكلية إمبريال كوليدج لندن.
• زميل الكلية الدولية لطب الأوعية الدموية في الولايات المتحدة الأمريكية.
الخبرة العملية
• المؤسس والمدير السابق لدى مركز صباح الأحمد للقلب.
• المدير السابق لقسم القلب والقسطرة التداخلية في مستشفى جابر الأحمد للقوات المسلحة.
• المدير السابق لقسم القسطرة التداخلية في مستشفى دار الشفاء.
• استشاري أمراض القلب والأوعية الدمويّة، مستشفى الصباح.
الجمعيات المهنية والمنظمات الدولية
• عضو في المجلس التنفيذي لشبكة مؤسسات القلب في آسيا والمحيط الهادي، والاتحاد العالمي للقلب.
• سبق أن شغلت أيضاً منصب نائب رئيس الشبكة.
• عضو في جمعية القلب البريطانية.
الجوائز
• مُنحت الدكتورة الحبيب جوائزَ مرموقةً، بما في ذلك «جائزة جون غودوين » The John Goodwin Award للتميُّز في أمراض القلب.
البحث
تحديد مصير مرضى التضخم في عضلة القلب إكلينيكيا ووراثيا وإشعاعيا في دولة الكويت
الدكتورة فريدة الحبيب
الباحث الرئيسي
استشاري أمراض القلب والأوعية الدمويّة
مستشفى الصباح – الكويت
الأستاذ الدكتور السير مجدي يعقوب
معهد مجدي يعقوب للأبحاث
إمبريال كوليدج لندن – المملكة المتحدة
الدكتورة ليلى بستكي
مديرة مركز الكويت للأمراض الوراثية – الكويت
الدكتورة بهية النفيسي
استشاري أشعة
قسم الرنين المغناطيسي
المستشفى الصدري – الكويت
المقدمة
د. فريدة محمد حبيب الحبيب معروفة بمساهماتها في أمراض القلب، و هي صاحبة مسيرة مهنية ممتدة على مدار عقود، تميَّزت بإنجازات رائدة، وتفانٍ في رعاية المرضى. اتسمت رحلة الحبيب بالسعي الدؤوب بحثاً عن المعرفة، والالتزام بتطوير طب القلب والأوعية الدموية. وقد حصلت على مؤ هلات علمية مرموقة، وهي عضو في عديد من المنظمات الطبية الرائدة،
ولها مساهمات بحثية جوهرية، ولذا فإن تأثير الدكتورة الحبيب هو تأثيرٌ ذو صدًى عالمي.
في هذه المقابَلة الحصرية، نعرض نتائج أحدث أبحاثها – المموَّل من مؤسسة الكويت للتقدم العلمي – حول حالة قلبية تُسمى ”اعتلال عضلة القلب التضخُّمي“ (Hypertrophic cardiomyopathy ، اختصاراً: اعتلال تضخُّم القلب HCM). هو اضطراب غامض، غالباً ما يتوارى في الظلال في كثير من الحالات غير المشخَّصة، ويؤدي إلى الموت القلبي المفاجئ في الشباب. وكان هدف هذا البحث هو تسليطَ الضوء على هذه الحالة الطبية، والكشف عن أُسسها الجينية وأعراضها الإكلينيكيّة، وكذلك
سماتها في التصوير بالأشعة.
لم يحدِّد البحث طفرات جينية جديدة مرتبطة بتضخم القلب HCM فحسب، بل كشف أيضاً عن ارتباط لم يُبلَغ عنه سابقاً بين تضخم القلب HCM ومتلازمة بروغادا Brugada Syndrome ، مما يُلقي ضوءاً جديداً على تعقيدات أمراض القلب. و هكذا لم تُوسع هذه النتائج المشهدَ الجيني للاعتلال HCM فحسب، بل مهدت الطريقَ أيضاً لتدخلات مبكرة تنقذ حياة المرضى، بما في ذلك غرْسُ مُقوِّم نظم القلب ومزيل الرجفان القابل للغرس (Implantable cardioverter defibrillator ، اختصاراً: المقوِّم
ICD)، لخفض خطر الموت القلبي المفاجئ (Sudden cardiac death) في الأفراد ذوي المخاطر العالية.
ما الذي دفعكِ إلى البحث في هذا المرض، وما أهدافُك النهائية من ناحية تأثيرِه في الرعاية الصحيّة؟
د. فريدة: على مر الأعوام، شهدت وحدةُ العناية التاجية في الكويت إدخالَ شباب إلى المستشفى لديهم تاريخ عائلي من الموت المفاجئ. مرض تضخم القلب HCM هو مرض وراثي يسببه وجود طفرة جينية واحدة. وهو يتبع نمطاً جسمياً سائداً ( Autosomal dominant pattern )، مما يعني أن وراثة نسخة واحدة فقط من الجين المتحور من أحد الوالدين يكفي لتطور الحالة المرضية. ومع ذلك ليس بالضرورة أن تظهر الأعراض على كل من يحمل الجين (أو ما يعرف اصطلاحاً ب”غير كامل النفاذ“ Incomplete penetrance )، وينتقل عبر العائلات، حيث تصبح عضلة القلب أكثر سمكاً من المعتاد. ويرتبط هذا المرض بالفسيولوجيا المَرَضية Pathophysiology المعقدة والسمات الإكلينيكية غير المتجانسة، لأنه ينطوي على تغييرات مختلفة في كيفية عمل القلب، ويظهر بشكل مختلف لدى الأشخاص المختلفين، مما يجعل من الصعب تشخيصه وعلاجه. وهو السبب الرئيسي للموت القلبي المفاجئ لدى الشباب. ويحدث في واحد لكل 500 شخص، وإن كانت عديدٌ من البيانات الحديثة تُبلغ عن واحد لكل 200.
ومع ذلك هناك نقص ملحوظ في المعلومات التفصيلية حول هذه الحالة المثيرة للقلق في الأدبيات المنشورة. إذ تظلّ أكثر من
50% من الحالات من دون تشخيص جيني؛ مما يشير إلى احتمال وجود مزيد من الجينات المؤدية إلى هذا المرض. إضافةً إلى ذلك تنقُصنا المعرفة الكافية عن خصائص الحالة وتركيبها الجيني في سكان الكويت، حيث تسود قرابة الدمّ Consanguinity بصورة كبيرة.
لقد شجَّعني عملي السابق مع الأستاذ الدكتور السير مجدي يعقوب مدة خمسة أعوام، واطلاعي على أبحاثه على السعي إلى التعاون مع إمبريال كوليدج Imperial College London لندن لإجراء اختبارات جينية على عينات دم مرضانا. لكن مع اندلاع جائحة كوفيد – 19 في العام الأول من الدراسة، تعاوناً مع د. ليلى بستكي، مديرة مركز الكويت للأمراض الوراثية (اختصاراً: المركز KMGC) – مبنى غنيمة الغانم للوراثة. وبذلنا كل جهدنا للحصول على المواد والأجهزة المناسبة لهذا النوع من الاختبارات الجينية، لإجراء تحليل يسمى سَلسَلة كامل الإكسوم Whole exome sequencing . نجحنا في نهاية المطاف في ضمان دقة التحليل والتأكد من عدم وجود فروق بسبب اختلاف الاختصاصيين المشرفين على التحليل، أو ما يعرف تقنياً بالتباين بين الراصدين Inter-observer variability.
ما أكبر العقبات التي واجهتكِ في مسيرتك المهنية بصورة عامة، وفي هذا المشروع البحثي بصورة خاصة وكيف تغلبتِ عليها؟
د. فريدة: عملت في مستشفيات مختلفة في بلدان مختلفة طَوال مسيرتي المهنية، بَدءاً من مستشفى ميامي جاكسون التذكاري
Miami Jackson Memorial Hospitalومستشفى كيمبريدج Cambridge Hospital في الولايات المتحدة الأمريكية، إلى مستشفى هامرسميث Hammersmith Hospital ومستشفى هيرفيلد Harefield Hospital في لندن، وانتهاءً بمركز صباح الأحمد لأمراض القلب في المستشفى الأميري، وعملي حالياً في مستشفى الصباح. وقد شكَّل هذا الاختلاف في الثقافات الاجتماعية والاقتصادية والوعي الصحي تحدياً لا عائقاً. ومع ذلك فإن ندرة المختصين بعلم الإحصاء الحيوي في الكويت كانت أكبر عقبة في مسيرتي المهنية، وهو التحدي الذي سلَّطنا عليه الضوء في هذا البحث. وكان الحلُّ الوحيد هو حضورَ دورات عبر الإنترنت في الإحصاء الحيوي، والاستعانة بمبرمج متخصص ببرنامج ستات فيو StatView، والتشاور مع خبراء إحصائيين خارج الكويت.
هل يمكنكِ توضيح أهمية مرض تضخُّم القلب HCM ومدى انتشاره في الكويت؟ ما الذي دفعك إلى البَدء في بحث يُركز تركيزاً خاصاً على هذه الحالة؟
د. فريدة: عملتُ مع مرضى مصابين بأمراض حرجة في معظم مسيرتي المهنية الطويلة، فتعرّفت على عديد من العائلات التي تعاني تضخم القلب HCM. لتحسين رعايتي الإكلينيكية، كنتُ في حا جة إلى وصف دقيق علمياً لهذا المرض في الكويت. من المعروف أن الأسباب الثانوية لتضخم البطين الأيسر left ventricular hypertrophy (اختصاراًً: التضخم LVH) شائعة لدى مرضى ارتفاع ضغط الدم الكويتيين، لكن السبب الجيني للتضخم LVH غير معروف جيداً.
تتطلب مهنتُنا اكتشافاتٍ ودراسات مستمرةً لفهم الفسيولوجيا المرَضية، وتحديد خصائص مرض معين لدى مجموعة سكانية معينة، كي نتمكن من تقديم العلاج الأمثل لها.
هلّا حدّثتِنا عن بعض المنهجيات أو التقنيات الرئيسية التي استُخدمت في بحثكِ، وكيف تُساهم في تعزيز فَهمنا لصحة القلب؟
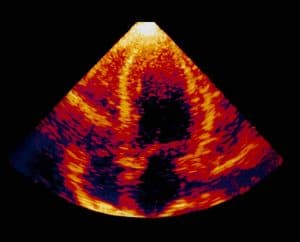
د. فريدة: امتدّت الدراسة 36 شهراً، بَدءاً من يناير 2021. وقد التزمنا فيها بأحدث التوصيات العالمية والإرشادات العلمية إلى (2023) التي وضعتها جمعيات القلب الأمريكية والأوروبية، وأجرينا جميع الاختبارات اللازمة وفقاً لذلك. في الزيارة الأولى للمريض، كنا نجمع البيانات الإكلينيكية باستخدام تخطيط القلب الكهربائي ECG، وجهاز هولتر للمراقبة Holter monitoring، وتخطيط صدى القلب Echocardiography، وفحوص التصوير بالرنين المغناطيسي MRI scan ، ونتائج التصوير الإشعاعي. جدولت الزيارات اللاحقة بناء على شدة المرض، واحتفظنا بسجلات لتوثيق حالات دخول المستشفى والأمراض المصاحبة والمضاعفات.
قدّم لنا استخدام تخطيط صدى القلب والتصوير بالرنين المغناطيسي للقلب في جميع الحالات (156)، بالإضافة إلى استخدام التصوير بالرنين المغناطيسي المعزز بالتباين بالغادولينيوم Gadolinium contrast MRI، بياناتٍ موسعةً عن ثخانة الجدار وموقع الثخانة (الجدران الأمامية والخلفية للحاجز Septum والقمة Apex) وعلاقته بتليف عضلة القلب Myocardial fibrosis. وفي حين أن الأدبيات المنشورة من الدراسات الجينية المتطورة السابقة تشير إلى أن نحو 50% من الحالات تحمل الجينات ذات الصلة، إلا أننا قد وثّقنا أنّ 58.7% من مرضانا يحملون الجين المسبِّب للمرض.
ما الاكتشافات الجينية المهمة التي توصلتِ إليها في بحثك، لا سيما فيما يتعلق بتضخم القلب HCM في العائلات التي يشيع فيها زواج الأقارب، وما الآثار المترتبة على هذا الاكتشاف بالنسبة إلى الفهم الأوسع لهذا المرض والأبحاث الجينية؟
د. فريدة: حدّدنا طفرة جينية جديدة، وهي تحورات متغيرات أو أشكال مختلفة من الجين في الجينات الموروثة من كلا الوالدين (متماثلة الألائل Homozygous variant) في موضع يُسمى ALPK3 ، فيها طفرة عبارة عن تغير يتسبب في إضافة حمض أميني مختلف (أو ما يعرف علمياً بطفرة مغلّطة) Missense فتسبب في نشوء المرض، وذلك في عائلة يسود فيها زواج الأقارب ولديها تضخم قلب HCM متنحٍّ Recessive ، أي لا يظهر المرض إلا عندما يرث الفرد جينين اثنين غير سائدين.
ومن المهم الإشارة إلى اكتشافنا لهذه الجينات الجديدة التي لم تدرس إلا نادرا، ولكنها مهمة مثل الجينات: BSCN و NEXN و ALPK3 في المرضى الذين يعانون اعتلالَ عضلة القلب الانسدادي التضخمي Hypertrophic Obstructive Cardiomyopathy (اختصاراً: مرض عضلة القلب HOCM). أُبلِغ عن ذلك في طفلين ماتا موتاً قلبياً مفاجئاً قبل أن يبلغا عمر المراهقة. ولحسن الحظ كان مريضنا متماثل ألائل ALKP3 في الأربعينيات من عمره وهو ابن لأبوين قريبين. وكان لاكتشاف وجود تليف عضلة القلب في بيانات التصوير بالرنين المغناطيسي تأثير كبير في فهم السمات الإكلينيكية لتضخم القلب HCM، وكذلك المسار المحتمل مصير للمرض Prognosis.
وهذا يؤكد ضرورة توسيع نطاق الأبحاث الجينومية لتشمل المجموعات التي يشيع فيها زواج الأقارب والتي لم تدرس إلّا قليلاً. سيساعد ذلك على الكشف عن تأثيرات التعبير عن التنوعين الجينيين الاثنين في الشخص (تنويعات الألائل الثنائيةBiallelic) والجينات المتنحية الجديدة في الشكل الظاهر (النمط الظاهري Phenotype) لمرض تضخم القلب HCM، مما سيسلط الضوء على جوانب مهمة لهذه الحالة.

كيف تساهم هذه النتائج في فَهمنا لأمراض القلب، وإمكانية التدخلات المبكرة للوقاية من الموت القلبي المفاجئ؟
د. فريدة: لم نحدد خلال بحثنا طفرات جينية جديدة مرتبطة بمرض تضخم القلب HCM فحسب، بل كشفنا أيضاً عن ارتباط لم يُبلَغ عنه سابقا بين الاعتلال HCM ومتلازمة بروغادا، مما يلقي ضوءاً جديداً على تعقيدات أمراض القلب.
كلا الرضين يسبب عدم انتظام دقات البُطين.
فدرسنا الارتباط الجديد بين المرضى الذين يعانون مرض تضخم القلب HCM ومتلازمة بروغادا. وهذه المتلازمة هي مرض جيني نادر وله سمات مميزة في تخطيط القلب الكهربائي. والمتلازمة مسؤولة عن 20 % من حالات الموت المفاجئ بسبب اضطرابات النظم البطينية Ventricular arrhythmia الخطيرة لدى الأفراد الأصحاء ذوي القلوب الطبيعية بنيوياً، وعن %4 من جميع أسباب الموت المفاجئ.
لم تُوسِّع النتائج التي توصلنا إليها المشهدَ الجيني لمرض تضخُّم القلب HCM فحسب، بل مهدت الطريق أيضاً لتدخلات مبكرة منقذة للحياة، بما في ذلك غرْسُ مُقوِّم ICD ، لتخفيض خطر الموت القلبي المفاجئ لدى الأفراد المعرضين لمخاطر عالية.
لم يُبلغ عن هذا الارتباط سابقاً، ويتطلب الأمر إجراء مزيد من الدراسات باستخدام
نماذج وأدوات جديدة في الطب الحيوي، إذ إن كلا المرضين سبب مهم للموت القلبي المفاجئ. وهذه النتيجة تُشير إلى ضرورة دراسة جين نادراً ما يُبلغ عنه.
وقد أنتجت هذه الدراسة قاعدةَ بيانات كبيرة للمرضى المصابين بمرض تضخم القلب HCM، والتي سيمكن لجميع الأطباء في الكويت استخدامُها في المستقبل. بشرح محدِّدات ونتائج مرض تضخم القلب HCM في الكويت، فإن بحثنا لا يسدُّ فجوة حرجة في الأدبيات فحسب، بل يمثلّ أيضاً أساساً للدراسات والمبادرات المستقبلية التي تهدف إلى تعزيز الكشف المبكر عن هذه الحالة المهددة للحياة وإلى تدبيرها، وآمل أن نتمكن من إنشاء قاعدة بيانات وطنية لتتبع جميع حالات مرض تضخُّم القلب HCM، مما سيحسِّن علاج المرضى، ويشجع البحث العلمي في المستقبل.
كيف ساهم التعاون بين وزارة الصحة ومؤسسة الكويت للتقدم العلمي في الكويت وجامعة إمبريال كوليدج لندن في توسيع نطاق بحث ونتائجه المحتملة؟
د. فريدة: في الواقع، اقتصر التعاون على العام الأول. وسط اندلاع جائحة كوفيد-19، نقلت شخصياً عينات الحمض النووي DNA إلى مختبرات الأستاذ دكتور السير مجدي يعقوب. وفي وقت لاحق، وعلى الرغم من التحديات، تمكّنا من الحصول على جميع المواد الكيميائية (الكواشف Reagent والإكسومات Exome) اللازمة لإجراء البحث في مركز الكويت للأمراض الوراثية.
ويُعرب الفريق عن امتنانه للسير مجدي يعقوب لتوجيهاته والنقاش المثمر. والأهم من ذلك أنني حضرت عمليات جراحية أجراها الأستاذ مجدي على مرضى تضخم القلب HCM. وهو رائد في هذا النوع من الجراحة النادر في العالم والجديد نسبياً. تتضمن العملية استئصال العضلة Myectomy جراحياً لتقليل حجم القلب بإزالة الأجزاء المتضخمة Hypertrophied من عضلة القلب Myocardium. وكان من الضروري بالنسبة إليَّ أن أشاهد هذه العمليات مباشرة كي أتمكن من شرحِها شرحاً شاملاً لمرضاي. إضافةً إلى ذلك ناقشت تقديم هذه الجراحة المهمة للفريق الجراحي الكويتي مع الدكتور جمال الفضلي، مدير مستشفى الأمراض الصدرية. وأبدى اهتماماً كبيراً ببَدء التدريب على هذه الجراحة وبناء القدرات لإجرائها في الكويت بدلاً من إرسال المرضى إلى الخارج.
هلّا وضحتِ النهجَ متعدد التخصصات المستخدم في مشروعك البحثي؟ وكيف يمكن لهذا النهج التعاوني تحسين رعاية المرضى ونتائج العلاج؟
د. فريدة: أدّى نهجُنا متعدد التخصصات، الذي ضّم أطباء قلب واختصاصيِّي أشعة وأطباء أطفال واختصاصيّي جينات، دوراً محورياً في كشف أسرار مرض تضخم القلب HCM وتوفير رعاية شاملة لمرضانا في الكويت. كان أطباء القلب يحيلون الحالات المحتملة إليَّ، فأقيِّمها بدقة لاستبعاد أي أسباب ثانوية لتضخم البطين باستخدام التقييمات الإكلينيكية، بما في ذلك تخطيط القلب الكهربائي وجهاز هولتر للمراقبة. وفي الوقت نفسه ، تُجري الدكتورة بهية النفيسي وفريقُها فحوصَ التصوير بالرنين المغناطيسي، بينما تولت الدكتورة ليلى بستكي وفريقُها التوصيف الجيني لجميع المرضى وعائلاتهم.
عقدنا اجتماعات تدقيق منتظمة للتحقق من صحة جميع التشخيصات بصورة دورية، إضافة إلى جلسات مع المرضى وإخوتهم وأقاربهم بعد إجراء تحليل شامل لجميع البيانات. هدفت هذه الاجتماعات إلى شرح خيارات العلاج المختلفة ومسار المرض. وعند الضرورة، أحلنا الأطفال إلى أطباء الأطفال.
هلّا شاركتِنا في أي لحظات لا تُنسى أو اختراق علمي حدث في أثناء بحثك؟
د. فريدة: في أحد اجتماعات التدقيق التي أجريناها، اكتشفنا علاقة جديدة لم يُبلغ عنها من قبل بين مرض تضخم القلب HCM ومتلازمة بروغادا، وهذه المتلازمة سبب آخر للموت القلبي المفاجئ. أثار هذا الاكتشاف خليط من المشاعر في داخلي – الإثارة في الكشف عن هذه العلاقة غير المعروفة سابقاً بين مرض تضخم القلب HCM ومتلازمة بروغادا، إلى جانب مشاعر الحزن والأسى عند مناقشة التأثيرات المترتبة على ذلك مع آباء الأشقاء الأصغر عمراً.
على سبيل المثال، أتذكر بوضوح حالةٌ تتعلق بصبي في السادسة من العمر ولا تظهر عليه الأعراض . كان من الصعب أن نشرح للعائلة ضرورة إجراء استقصاءات مثل اختبار عقار الفليكاينيد Flecainide test وغرس جهاز داخل القلب لاحقاً للوقاية من الموت المفاجئ. تطلّبت هذه التجربة العاطفية تواصلاً حساساً، واستخدام لغة متحفظة، والتحدث بلين للتأكد من فَهمهم للتشخيص وخيارات العلاج ومسار المرض. و تطلب الأمر توفير دعم نفسي مُكثَّف لكل من الأسرة والطفل.
هلّا توسعتِ في أهمية نتائج بحثك فيما يتعلق بملف مريض مرض تضخم القلب HCM، بصورة خاصة في سياق السكان الكويتيين، الذين لم تكن البيانات متوافرة عنهم سابقاً؟
د. فريدة: كشف هذا البحث عن مجموعة جديدة من المرضى المعرضين لخطر الموت المفاجئ بسبب اضطرابات النظم الخطيرة، مما سيسمح لنا بحمايتهم حمايةً استباقية، بغرس المقومات ICD في عمر مبكر غالباً.
وبالمثل، فإن حديد وجود تليف في عضلة القلب بالتصوير بالرنين المغناطيسي متأخر التعزيز بالغادولينيوم Late gadolinium enhancement MRI، أثّر تأثيراً كبيراً في قرارات علاج المريض وسهَّل اختيار طرق علاج حثيثة Aggressive treatment مثل استئصال العضلة الجراحي. مع أنَّ هذا النهج جديد نسبياً ولايُتَّبع إلا في عدد قليل من المراكز، أرسلنا سبعة مرضى إلى الخارج لهذا الإجراء، وكانت نتائجهم واعدة جداً. ومن ثمّ، فإن هذا البحث يضع أساساً متيناً لإدخال هذه الجراحة إلى الكويت، مما قد ينقذ الأرواح، بصورة خاصة في الحالات الشديدة.
إضافةً إلى ذلك، يقدّم البحث رؤى حول معالجة قضية زواج الأقارب داخل الأسر المصابة في الكويت، الذي يزيد خطر إنجاب أطفال متأثرين بالمرض. ويمكن لهذا البحث أن يرفع الوعي العام بالاكتشاف المبكر للمرض والعلاج المبكر قبل أي حدث مأساوي.
هل من كلمات أخيرة؟
د. فريدة: يسعدني أن أشارك هذه النتائج. وأُقدم جزيلَ الشكر لمؤسسة الكويت للتقدم العلمي وإدارة البحوث والتكنولوجيا على تعاوُنهما الاستثنائي واحترافيتهما. أنا ممتنة للأستاذ الدكتور السير مجدي يعقوب، والدكتورة أمينة فرحان المدير العام لمؤسسة الكويت للتقدم العلمي، لتوجيهاتهما. وأحمل تقديراً خاصاً للدكتورة ليلى بستكي، والدكتورة بهية النفيسي، وصبحي حسين، وأحمد سليم من وزارة الصحة.
النتائج:
• أدت نتائج هذا البحث إلى إنشاء مركز التميز Center of Excellence in Kuwait في الكويت للتدبير الإكلينيكي والعلاجي للمرضَى الذين يعانون اعتلالاتِ عضلة القلب الوراثية Inherited cardiomyopathy . كان النهج المتَّبع في تدبير المرضى في المشروع نهجاً متعدد التخصصات، ويتضمن العمل التعاوني مع أطباء القلب، واختصاصيِّي الأشعة، وأطباء الأطفال، واختصاصيِّي الجينات، وغيرهم.
• حدّد فريق البحث الأساس الجيني للمرض لدى السكان الكويتيين بتضمين 56 مريضاً غير كويتي في المجموعة المكونة من 100 مريض كويتي، مما يجعل العدد الإجمالي 156. مثّلت هذه المجموعة تنوع السكان الكويتيين. وحدّد البحث الطفرات المرتبطة والنمط الجيني Genotype والنمط الظاهري الناجم عنه المتصلَين، واكتشف الفريق أيضا 3 جينات جديدة، هي TRIM63 و BSCN و ،ALPK3 والتي نادراً ما توصف في الأدبيات.
• اكتشف البحث علاقة جديدة بين الاعتلال HCM ومتلازمة بروغادا، وهو ما لم يُبلَغ عنه من قبل.
• شملت المحدِّدات المحتملة التي فُحصت كلا من النمط الجيني، ومدى التضخم وموقعه المحدد بتخطيط صدى القلب والتصوير بالرنين المغناطيسي، ومدى التليف المحدد بالتصوير بالرنين المغناطيسي متأخر التعزيز بالغادولينيوم.
• درس الفريق أيضاً عملية موسعةً لاستئصال جزء من العضلة القلبية في مجموعة فرعية مكونة من سبعة مرضى كويتيين يعانون حالاتٍ انسداديةً، وخضعوا لتدخل جراحي هذا العام (2024).




